Nouvelles solutions pour la dialyse péritonéale : pourquoi en avons-nous besoin et de quoi s'agit-il ?
DOI :
https://doi.org/10.25796/bdd.v8i2.87078Mots-clés :
dialyse péritonéale, solutions biocompatibles, toxicité du glucose, xylitol, L-carnitine, alanine-glutamineRésumé
Les solutions de dialyse péritonéale (DP) génèrent des gradients de concentration et d'osmose à travers la membrane péritonéale afin d'éliminer les toxines urémiques et de réaliser l'ultrafiltration. L'utilisation des solutions de dialyse actuelles entraînent également des processus péritonéaux et systémiques pro-inflammatoires, pro-fibrotiques et pro-angiogéniques qui pourraient être liés aux résultats des patients. Les causes les plus fréquentes d'échec de la technique de DP étant la mortalité, les infections, la clairance insuffisante des solutés et l'échec de l'ultrafiltration, il est important de réfléchir aux effets et au pouvoir modificateur des compositions des solution de DP.
Cet article traite des effets péritonéaux et systémiques des solutions de DP à base de glucose et des preuves de l'utilisation d'alternatives à base d'icodextrine et d'acides aminés. Les innovations récentes en matière de solutions de DP tentent de surmonter les toxicités péritonéale et systémique des formulations actuelles en utilisant un agent osmotique alternatif et/ou en contrecarrant les effets métaboliques de la charge en hydrates de carbone par la solution de DP.
Introduction
Les solutions de dialyse péritonéale (DP) génèrent un gradient de concentration à travers la membrane péritonéale permettant la diffusion des toxines urémiques de la circulation du patient vers sa cavité péritonéale. La diffusion étant un processus bidirectionnel, les petites molécules contenues dans le liquide de DP seront également absorbées par le patient en DP. Le gradient osmotique exercé par le liquide de DP permet, quant à lui, à l’eau de traverser la membrane péritonéale. L’application des principes physiques de diffusion et d’osmose par un liquide de DP séjournant dans la cavité péritonéale permet de gérer la clairance et le volume du patient en DP.
La DP offre une survie globale similaire à celle de l’hémodialyse en centre, avec une tendance à un avantage de survie pour les patients en dialyse péritonéale dans les premières années suivant le début de la dialyse [1][2]. Néanmoins, la survie globale des patients reste faible avec une probabilité de survie de seulement 47% ,5 ans après le début de la dialyse [1]. Chez les patients en dialyse, l’échec de la technique de DP n’est pas rare, avec des taux d’échec de la technique de DP censurés par les décès à 1 et 2 ans de 23 % et 35 % respectivement dans une cohorte européenne contemporaine [3]. Les causes les plus fréquentes d’échec de la technique de DP après décès sont les infections, une clairance insuffisante et/ou des problèmes d’ultrafiltration [3].
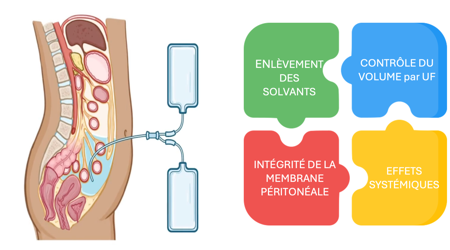
Cet article décrit la composition des solutions de dialyse de DP et leurs effets péritonéaux et systémiques. Bien que l’objectif principal des solutions de dialyse de DP soit de servir à l’élimination des solutés et à l’ultrafiltration , ces solutions jouent également un rôle dans l’intégrité de la membrane péritonéale, et l’absorption systémique des solutés de dialyse de DP influe sur les voies métaboliques systémiques. Nous discutons de la manière dont les nouveaux développements en matière de solutions de dialyse de DP surmontent leurs inconvénients de l’ère actuelle, et dont les innovations en matière de solutions de dialyse de DP visent à optimiser le résultat composite de la clairance des solutés, de l’ultrafiltration, des changements de la membrane péritonéale au fil du temps sur la DP et des effets systémiques par la solution (Figure 1).
Figure 1.Les solutions de dialyse péritonéale servent à l’élimination des solutés et à l’ultrafiltration. Les solutions de dialyse de DP affectent également l’intégrité de la membrane péritonéale et l’absorption systémique des solutés de DP influence les voies métaboliques systémiques. Les innovations en matière de solutions de dialyse de DP visent à optimiser le résultat composite de la clairance des solutés, de l’ultrafiltration, des modifications de la membrane péritonéale au fil du temps sur la DP et des effets systémiques du fluide de DP.
Solutions de dialyse péritonéale de première génération
Les solutions de DP de première génération, également appelées solutions conventionnelles de DP, contiennent des électrolytes, un tampon et du glucose comme principal agent osmotique (Tableau I). La teneur en glucose de ces solutions est 10 à 50 fois supérieure à la concentration de glucose dans le plasma. Le processus de stérilisation à la chaleur des solutions de DP entraîne la production de produits de dégradation du glucose (PDG), bien qu’il soit effectué à un pH faible. Les solutions de DP conventionnelles sont donc caractérisées par un pH faible, une teneur élevée en glucose et une forte teneur en PDG.
Une étude de référence publiée en 2002 a mis en évidence des lésions histopathologiques significatives de la membrane péritonéale au fil du temps avec l’utilisation de ces solutions conventionnelles de DP. Après une exposition prolongée à des liquides à faible pH, à haute teneur en glucose et à haute teneur en PDG, les évaluations histopathologiques de suivi de la membrane péritonéale des patients ont montré une perte de cellules mésothéliales, un épaississement sous-mésothélial, une angiogenèse et une vasculopathie péritonéale [4]. Au début des années 2000, il a également été reconnu que le transport péritonéal de solutés augmentait avec la durée du traitement chez une partie des patients en DP et que cette augmentation était associée à une exposition péritonéale plus importante au glucose hypertonique [5]. Bien que le changement de l’état du transport des solutés au fil du temps soit associé à l’exposition au glucose, les changements fonctionnels et histopathologiques au sein de la membrane péritonéale induits par l’utilisation de solutions de DP à pH faible, à glucose élevé et à PDG élevé ont orienté l’»hypothèse de biocompatibilité des solutions de DP». L’hypothèse de biocompatibilité suggère que des dommages péritonéaux morphologiques et fonctionnels peuvent être causés par les solutions de DP conventionnelles - solutions de DP à faible pH, à forte teneur en glucose et à forte teneur en PDG - et que ces changements peuvent être atténués par des solutions de de deuxième génération, dites biocompatibles.
| Référence plasmatique (adulte) |
Fluide à base de G% de première génération (Solutions à faible pH et à PDG élevé) |
Fluide à base de G% de deuxième génération (Solutions à pH neutre et à faible PDG.) |
Solution d’acides aminés | Icodextrine | |
| Électrolytes (mmol/L) | |||||
| Sodium | 136-145 | 132 | 132-134 | 132 | 133 |
| Calcium | 1.12-1.32 | 1.25/1.75 | 1.25-1.75 | 1.25 | 1.75 |
| Magnésium | 0.65-1.05 | 0.25/0.75 | 0.25/0.5 | 0.25 | 0.25 |
| Chlorure | 98-107 | 95/102 | 95-104 | 105 | 96 |
| Potassium | 3.5-5.1 | 0 | 0 | 0 | 0 |
| Tampon (mmol/L) | |||||
| Acétate | 0 | ||||
| Lactate | 0.5-2 | 40/35 | 10-15/35/0 | 40 | 40 |
| Bicarbonate | 22-28 | 25/0/34 | |||
| pH | 7.4 | 5.5 | 7.0-7.4 | 6.7 | 5.5 |
|
Agent osmotique (g/dL) (osmolalité) | |||||
| Glucose |
0.05 - 0.1 (280-300) |
1.36/2.27/3.86 (347/398,486) |
1.36-1.5/2.27-2.5/3.86-4.25 (350/397/490) |
||
| Acide aminé |
0.05 - 0.1 (280-300) |
1.1 (365) |
|||
| Icodextrine |
7.5 (284) |
||||
| (PDG: produits de dégradation de glucose) | |||||
Solutions de dialyse péritonéale de deuxième génération
Pour diminuer la toxicité des solutions de DP à faible pH, à forte teneur en glucose et à PDG élevés sur la membrane péritonéale, des poches à plusieurs compartiments ont été mises au point, permettant de stériliser séparément le glucose à un pH très bas, générant ainsi moins de PDG. Avant utilisation, le compartiment à glucose est mélangé avec le(s) autre(s) compartiment(s) de la solution de DP contenant des électrolytes et un tampon. Après mélange des différents compartiments de la poche de DP, on obtient une solution de DP à pH neutre contenant moins de PDGs par rapport aux solutions de première génération. Les solutions de DP de deuxième génération se définissent donc par leur pH neutre et leur moindre teneur en PDG et sont des solutions dites biocompatibles (Tableau I).
Des études précliniques in vitro et in vivo utilisant des solutions de DP de deuxième génération ont montré des effets histopathologiques prometteurs avec une réduction des lésions mésothéliales induites par le fluide biocompatible, une réduction de la transition épithélio-mésenchymateuse (EMT), une réduction du dépôt de PDG, une réduction de la fibrose et de l’angiogenèse sous-mésothéliales et une réduction de la progression de la vasculopathie avec une meilleure préservation du glycocalyx endothélial [6][7][8][9]. En outre, les données observationnelles en pratique clinique au Japon suggèrent que l’utilisation de solutions de DP biocompatibles contribue à réduire le développement de la sclérose péritonéale encapsulée, stade ultime des modifications histopathologiques de la membrane péritonéale [10][11]. Cependant, les preuves des bénéfices cliniques sont encore débattues. Les résultats des essais cliniques contrôlés randomisés et des méta-analyses comparant les effets des solutions de DP biocompatibles par rapport aux solutions de DP conventionnelles sont moins clairs. Globalement, l’utilisation de liquides biocompatibles de deuxième génération est associée à une meilleure préservation de la fonction rénale résiduelle et du débit urinaire, bien que ces changements puissent être secondaires à une diminution de la capacité d’ultrafiltration. Par ailleurs, aucune amélioration de la fonction de la membrane péritonéale n’a pu être démontrée en utilisant des solutions de DP de deuxième génération [12][13][14].
Chez 24 enfants traités uniquement par des liquides de DP de deuxième génération, des biopsies péritonéales en série ont montré une activation précoce des fibroblastes, une néoangiogenèse et une vasculopathie. Chez ces enfants, la densité microvasculaire et les taux de transport péritonéal (D/P créatinine à 2 heures) étaient bien corrélés [15]. Ces données démontrent que les solutions biocompatibles peuvent entraîner une inflammation précoce, une transition épithéliale-mésenchymateuse, un épaississement sous-mésothélial, une angiogenèse et une vasculopathie chez les patients pédiatriques.
L’absence de bénéfices cliniques liés à l’utilisation de solutions à pH neutre et à faible PDG et la persistance de modifications histopathologiques et fonctionnelles de la membrane péritonéale induites par l’utilisation de ces solutions dites biocompatibles ont balayé l’hypothèse de la biocompatibilité. Une concentration de glucose non physiologiquement élevée, une caractéristique commune aux solutions de DP de première et de deuxième génération, a conduit à l’élaboration de l’»hypothèse du glucose».
L’hypothèse du glucose : effets systémiques et péritonéaux de l’exposition au glucose
Au cours d’un séjour en DP utilisant des solutions de DP de première ou deuxième génération, le transport bidirectionnel de solutés à travers la membrane péritonéale conduit à l’absorption systémique de glucose. On estime que l’absorption systémique quotidienne de glucose varie entre 90 et 300 g [16][17], ce qui représente une charge calorique importante, augmentant par la suite la masse grasse et la dyslipidémie. L’augmentation du glucose plasmatique et des PDG, secondaire à la diffusion à partir du liquide du DP vers la circulation du patient, favorise la formation de produits finaux de glycosylation avancée (AGE) dans le plasma et conduit à des effets cytotoxiques induits par le glucose [18][19]. La cytotoxicité du glucose est liée à plusieurs perturbations moléculaires. Tout d’abord, les AGE se lient à leurs récepteurs (RAGE) et induisent des effets inflammatoires et pro-angiogéniques par la génération d’espèces réactives de l’oxygène et par la libération de cytokines et de facteurs de croissance. Le glucose déclenche également une signalisation intracellulaire via la protéine kinase C et les voies des polyols, et l’hyperglycémie intracellulaire provoque des perturbations métaboliques entraînant une augmentation du rapport NADH/NAD+ , un état connu pour être induit par un apport insuffisant d’oxygène. Cette pseudo-hypoxie induite par le glucose provoque l’expression du facteur inductible par l’hypoxie, ce qui entraîne une augmentation des gènes codant pour des facteurs profibrotiques et angiogéniques tels que le facteur de croissance de l’endothélium vasculaire (VEGF) et le facteur de croissance transformant bêta (TGF-β), contribuant ainsi à l’angiogenèse et au dépôt de la matrice extracellulaire [20][21][22]. Les effets cytotoxiques du glucose entraînent donc des changements pro-inflammatoires, pro-fibrotiques et pro-angiogéniques, qui sont évidents dans la membrane péritonéale exposée aux solutions DP [4][15].
Nouvelles approches thérapeutiques
Les progrès récents dans le domaine des solutions de DP se sont concentrés sur des stratégies visant à contrecarrer la toxicité péritonéale et systémique des solutions de DP à base de glucose. Deux stratégies principales ont ainsi vu le jour :
(i) L’approche osmotique qui consiste à remplacer le glucose par un autre agent osmotique.
(ii) L’approche métabolique selon laquelle la solution de DP est complétée par un ou plusieurs agents qui atténuent les effets métaboliques de l’exposition au glucose.
Avant d’aborder les nouveaux développements en matière de solutions de DP, nous évoquons tout d’abord les alternatives aux solutions de DP à base de glucose déjà disponibles dans le commerce.
En général, il faut reconnaître qu’une cytotoxicité résiduelle par des mécanismes non liés au glucose ou aux produits de dégradation du glucose est possible. La toxicité liée au tampon a été suggérée dans des études évaluant la cytotoxicité de différents liquides à base de glucose [23]. De même, des modifications de la membrane péritonéale liées à la tonicité ou à l’osmolalité ont été décrites dans des études précliniques, sans lien avec la pseudohypoxie induite par un taux élevé de glucose [24][25][26]. L’identification de ces voies contribuera à compléter le tableau de ce qui rend un liquide réellement biocompatible.
Solutions de remplacement des liquides de DP à base de glucose
disponibles dans le commerce
L’icodextrine est un polymère de glucose à haut poids moléculaire dérivé de l’amidon, utilisé dans la dialyse péritonéale comme alternative au glucose. Sa taille moléculaire plus importante fait qu’il est moins facilement absorbé que le glucose. Après avoir pénétré dans la circulation, l’icodextrine est métabolisée en oligosaccharides plus petits tels que le maltose, le maltotriose et le maltotétraose. À ce jour, aucune donnée histopathologique sur les effets de l’utilisation de l’icodextrine au cours de la DP n’a été publiée. Des études cliniques, y compris des essais contrôlés randomisés, montrent une amélioration de l’ultrafiltration avec un meilleur contrôle de l’état volémique lors de l’utilisation de l’icodextrine, en particulier chez les patients dont le transport membranaire péritonéal est rapide et chez ceux qui n’atteignent pas les objectifs d’ultrafiltration et qui présentent un risque de surcharge volémique [27][28]. Le remplacement d’une demeure de glucose par l’icodextrine a montré une meilleure sensibilité à l’insuline chez les patients en dialyse traités par DP [29]. Chez les patients en dialyse péritonéale et traités par DP, une prescription de DP épargnant le glucose en utilisant de l’icodextrine et des solutions de DP à base d’acides aminés a amélioré les résultats de l’HbA1c [30]. Ces données confirment que la réduction de l’exposition au glucose pendant la DP diminue les effets systémiques de l’absorption de glucose associée à la DP. Il faut reconnaître qu’à ce jour, le plus grand nombre de preuves sur l’utilisation de solutions de DP sans glucose concerne l’icodextrine, avec un signal clair de sécurité et d’efficacité. De futures recherches sur les résultats centrés sur le patient et le rapport coût-efficacité associés à l’icodextrine sont nécessaires.
Les solutions DP à base d’acides aminés sont des solutions composées d’électrolytes, d’un tampon et d’un mélange d’acides aminés comme agent osmotique. Les solutions de DP à base d’acides aminés ont été développées pour optimiser l’état nutritionnel des patients en dialyse péritonéale. Les données précliniques sur la cytotoxicité de la membrane péritonéale sont limitées et contradictoires, et aucune donnée histopathologique décrivant les effets des solutions de DP à base d’amino-acides sur la membrane péritonéale n’est disponible à ce jour [8][31]. La pertinence clinique en termes d’amélioration de l’état nutritionnel par l’utilisation à long terme de liquides de DP à base d’acides aminés est limitée, car seul un essai à court terme (7 jours de suivi) de petite taille (8 patients) a été publié, montrant une légère amélioration de la cinétique des protéines [32].
Au total, l’utilisation de solutions de DP à base de glucose reste indispensable pour une prescription de DP à dose complète. Malgré la maximisation de l’utilisation des solutions de DP à base d’icodextrine et d’acides aminés dans la prescription de DP, les patients continuent d’être exposés à une absorption importante d’hydrates de carbone, à une exposition au glucose et à une absorption de PDG [33].
Nouveaux agents osmométaboliques prometteurs
La L-carnitine est un composé osmotiquement et métaboliquement actif, essentiel au métabolisme des acides gras et à la fonction mitochondriale, dont le poids moléculaire est similaire à celui du glucose. Elle est très soluble dans l’eau et chimiquement stable dans une solution aqueuse et convient donc à une utilisation en DP. Des études précliniques in vitro et in vivo ont démontré une amélioration de la survie des cellules endothéliales, une augmentation de l’expression de l’aquaporine-1 sur les cellules endothéliales et une réduction de la cytotoxicité induite par le glucose lorsque les solutions de DP étaient supplémentés en L-carnitine [34][35]. Il est rassurant de constater que les solutions équimolaires de glucose et de L-carnitine entraînent une ultrafiltration nette comparable, les solutions supplémentés en L-carnitine provoquant moins de lésions mésothéliales et moins d’altérations vasculaires [34][35]. Une étude clinique a randomisé 35 patients en dialyse traités par DP entre une prescription de DP avec des liquides de jour à base de glucose et des liquides de jour à base de glucose supplémentés en L-carnitine à 0,1 %, pour une période de traitement de 4 mois. Les deux groupes ont reçu de l’icodextrine pendant la nuit. La sensibilité à l’insuline s’est améliorée chez les patients en dialyse péritonéale sous DP supplémentée en L-carnitine [36]. Il est important de noter que la supplémentation en L-carnitine a été bien tolérée et que la fonction de la membrane péritonéale n’a pas changé d’un groupe à l’autre. Chez les patients en DP supplémentés en L-carnitine, le débit urinaire n’a pas changé, alors que les patients en DP du groupe témoin ont perdu significativement leur diurèse au cours de la période d’étude. La diurèse osmotique induite par l’absorption de L-carnitine est suggérée comme étant la cause du maintien du débit urinaire dans le groupe d’intervention [36].
Le xylitol est un sucre à 5 carbones utilisé comme substitut du sucre dans la nutrition parentale. Il s’agit d’un composé osmotiquement actif à faible indice glycémique qui entraîne une augmentation plus lente et plus faible du taux de glucose plasmatique et une moindre stimulation de l’insuline par rapport à l’absorption du glucose. Un essai clinique ancien, publié en 1982, a montré une réduction de 50 % des besoins en insuline et une amélioration des paramètres métaboliques lorsque 6 diabétiques insulinodépendants ont reçu 1,5 % et 3,0 % de xylitol en DP par rapport à des DP à base de glucose [37].
Récemment, l’utilisation combinée de 0,7 % ou 1,5 % de xylitol avec 0,02 % de L-carnitine et 0,5 % de glucose a été étudiée (Tableau II).
| Référence plasmatique (adulte) | Xylitol - L-carnitine - Glucose | |
| Électrolytes (mmol/L) | ||
| Sodium | 136-145 | 132 |
| Calcium | 1.12-1.32 | 1.3 |
| Magnésium | 0.65-1.05 | 0.5 |
| Chlorure | 98-107 | 101 |
| Potassium | 3.5-5.1 | 0 |
| Tampon (mmol/L) | ||
| Lactate | 0.5-2 | 35 |
| pH | 7.4 | 6.5-7.5 |
| Agent osmotique (g/dL) (osmolalité) | ||
| Xylitol | 0.7/1.5/2.0 | |
| L-Carnitine | 0.02 | |
| Glucose | 0.05 - 0.1 | 0.5/0.5/1.5 |
| Osmolalité | 280-300 | 346.5/399.1/480.8 |
In vitro, un liquide de DP contenant une faible dose de glucose, de L-carnitine et de xylitol a amélioré la viabilité cellulaire des cellules endothéliales de la veine ombilicale humaine de mères avec ou sans diabète gestationnel, a amélioré la viabilité des cellules mésothéliales humaines et a mieux préservé l’intégrité de la couche de cellules mésothéliales par rapport aux liquides de DP à base de glucose [38][39]. Fait important, la faible dose de glucose contenue dans ce liquide de DP n’a pas eu les effets histopathologiques délétères des concentrations plus élevées de glucose dans les liquides de DP de première et de deuxième génération [39]. Une étude ouverte de phase 2 récemment publié a comparé la sécurité et la tolérance du liquide de DP xylitol - L-carnitine - glucose à une prescription de DP classique à base de glucose et d’icodextrine chez 10 patients en DPCA sur une période de 4 semaines. L’utilisation du xylitol - L-carnitine - glucose a été bien tolérée et les patients n’ont pas ressenti de douleur ou d’inconfort lors de la perfusion.
L’adéquation et les caractéristiques de transport péritonéal n’ont pas été identifiées comme différentes entre les groupes [26]. Actuellement, une étude contrôlée randomisée de phase 3 avec évaluation des résultats en aveugle est en cours de recrutement en Italie, au Danemark, en Suède, au Royaume-Uni, en Allemagne et en Espagne (essai ELIXIR, NCT03994471 [40]). Cette étude vise à randomiser 170 patients en DPCA entre un régime DP standard utilisant 1 à 3 échanges journaliers à base de glucose et d’icodextrine pendant la nuit et 1 à 3 échanges journaliers utilisant 0,7-1,5% de xylitol, 0,02% de L-carnitine et 0,5% de glucose et d’icodextrine pendant la nuit, pendant 6 mois. Le critère d’évaluation principal est la non-infériorité en ce qui concerne le Kt/Vuréehebdomadaire. Les critères d’évaluation secondaires comprennent l’ultrafiltration péritonéale sur 24 heures, la fonction rénale résiduelle, le débit urinaire, les paramètres métaboliques des lipides et du glucose, les mesures des résultats rapportés par les patients et la sécurité [40]. La collecte des données devrait s’achever à la fin de l’année 2025.
De faibles taux de glutamine dans la cavité péritonéale au cours de la DP sont associés à une cytotoxicité liée à une réduction des modifications protéiques post-traductionnelles dépendantes de la glutamine (appelée O-GlcNAcylation) [41]. La supplémentation en glutamine des solutions de DP à base de glucose permet une cytoprotection médiée par la protéine de choc thermique. La supplémentation des solutions de DP à base de glucose avec le dipeptide alanine-glutamine permet la libération de glutamine dans la cavité péritonéale. Des études in vitro, in vivo et pilotes ont démontré une meilleure survie des cellules mésothéliales, des dommages moins importants aux cellules endothéliales et une meilleure préservation de la barrière péritonéale lorsque les solutions de dialyse à base de glucose étaient supplémentés avec le dipeptide alanine-glutamine libérant de la glutamine, par rapport à l’absence de supplémentation [41][42][43][44][45][46][47]. Ces études ont également montré une amélioration de la fonction immunitaire de la membrane péritonéale, une réduction du stress oxydatif et un rétablissement des réponses au stress [41][42][43][44][45][46][47]. Une étude croisée randomisée et contrôlée de phase 2 menée chez 6 patients en DP a comparé les effets de liquides de DP supplémentés en alanine-glutamine à ceux de liquides de DP supplémentés en placebo sur une période de 8 semaines. Les résultats ont montré une amélioration des marqueurs de l’intégrité de la membrane péritonéale, une réduction de l’inflammation systémique et une amélioration de la compétence immunitaire de la membrane péritonéale [48].
Les cellules mésothéliales expriment à la fois le cotransporteur sodium/glucose SGLT1 et le SGLT2, et il est donc pertinent d’évaluer les effets de l’utilisation des inhibiteurs du SGLT1/2 dans la DP. En effet, l’inhibition de l’absorption du glucose à travers la membrane péritonéale par l’inhibition du transport du glucose médié par le SGLT1/2 pourrait diminuer la toxicité locale et systémique liée au glucose tout en maintenant le gradient osmotique et en améliorant ainsi la capacité d’ultrafiltration. Des études in vitro ont montré que l’empagliflozine et la dapagliflozine réduisent la fibrose péritonéale et la transition épithéliale-mésenchymateuse [49][50][51][52]. Des études animales avec administration intrapéritonéale de dapagliflozine ont montré des améliorations de l’intégrité de la membrane péritonéale et l’administration entérique d’empagliflozine a réduit l’absorption du glucose et protégé contre la transition épithéliale-mésenchymateuse induite par le glucose [50][51][53][54]. Cependant, des données supplémentaires suggèrent que le transport médié par le SGLT1 pourrait être plus important pour faciliter le transport péritonéal du glucose que le SGLT2 [55]. L’essai EMPOWERED (jRCTs051230081) est un essai croisé randomisé en double aveugle contre placebo qui recrute actuellement 36 patients japonais souffrant d’insuffisance cardiaque et traités par DP pour deux périodes de traitement de 8 semaines de dialyse péritonéale complétées soit par de l’empagliflozine par voie orale, soit par un placebo. Le critère d’évaluation principal de l’étude est le changement du volume d’ultrafiltration quotidien entre le début de l’étude et la semaine 8 [56]. D’autres essais contrôlés randomisés évaluant les effets des inhibiteurs du SGLT2 chez les patients en dialyse péritonéale évaluent les taux de peptide natriurétique cérébral comme critère principal (jRCT1011210022), l’absorption du glucose dans le liquide de DP (NCT05671991) ou l’efficacité et la sécurité réno- et cardioprotectrices (NCT05374291).
Le 2-désoxyglucose est un analogue synthétique du glucose qui inhibe la glycolyse et contrecarre ainsi la signalisation profibrotique médiée par le TGF-β1. Des études in vitro ont montré que la supplémentation du liquide de DP avec du 2-désoxyglucose a amélioré la survie des cellules mésothéliales, a réduit les changements fibrotiques et a amélioré l’intégrité de la barrière mésothéliale et endothéliale péritonéale [57][58]. La validation clinique est en cours.
La taurine, le polyglycérol hyperbranché, le lithium et les glycosides de stéviol sont d’autres molécules faisant l’objet d’études précliniques. Toutes ont démontré une protection de la membrane péritonéale in vitro et dans des modèles animaux, mais les données d’essais cliniques font défaut [59][60][61][62].
Il convient de noter que des solutions de DP adaptées ont été étudiées ces dernières années, telles que les polymères de glucose à faible polydispersité, la DP bimodale combinant osmose cristalloïde et osmose colloïdale, les solutions de DP à faible teneur en sodium et sans sodium. Bien que ces modifications puissent réduire l’absorption des glucides et augmenter l’élimination du sodium, elles n’éliminent pas l’exposition au glucose, ce qui suggère un rôle potentiel de protection métabolique complémentaire [63][64][65].
Conclusion
La solution de DP idéale doit assurer une clairance efficace des solutés, une ultrafiltration, préserver l’intégrité de la membrane péritonéale et limiter la toxicité systémique. Les liquides de DP à base de glucose, bien qu’efficaces pour assurer l’élimination des solutés et de l’eau, contribuent à endommager la membrane péritonéale et à provoquer des complications systémiques. Les liquides de DP à base d’acides aminés et d’icodextrine offrent la possibilité de réduire l’exposition au glucose et la toxicité locale et systémique qui en découle ; cependant, ils n’éliminent pas le besoin de liquides de DP à base de glucose. Les solutions de DP osmométaboliques émergents combinant xylitol, L-carnitine et glucose à faible dose ou les solutions de DP supplémentées en alanine-glutamine sont les plus prometteuses pour mieux préserver l’intégrité de la membrane péritonéale et réduire la toxicité systémique du fluide de DP tout en maintenant une élimination adéquate des solutés et de l’eau par rapport aux solutions de DP à base de glucose.
Les stratégies visant à réduire la toxicité du glucose liée à la DP, y compris les adjuvants métaboliques et les inhibiteurs du SGLT, représentent une frontière de recherche en pleine évolution. Les cliniciens, les chercheurs et l’industrie doivent s’engager dans une collaboration structurelle pour accroître les connaissances sur la toxicité des solutions liée à la DP, pour rechercher les solutions existantes et pour soutenir les nouveaux développements. En l’absence d’une implication fiable de l’une ou l’autre partie, les possibilités d’améliorer les résultats des patients traités par dialyse péritonéale seront retardées.
Contributions des auteurs
Les auteurs déclarent qu’aucun outil d’intelligence artificielle générative n’a été utilisé pour la rédaction de ce manuscrit.
La conception du manuscrit a été réalisée par KF. CS et KF ont rédigé le manuscrit. FVH et FJ ont révisé le manuscrit et en ont fait un examen critique.
Tous les auteurs ont approuvé la version finale anglaise et française du manuscrit soumis au BDD.
Financement
Les auteurs n’ont reçu aucun financement pour la rédaction de cet article.
Numéro ORCID
Celeste Smeys : https://orcid.org/0000-0003-3924-6764
Freya Van Hulle : https://orcid.org/0000-0001-7079-4705
Florine Janssens : https://orcid.org/0009-0004-2863-6155
Karlien François : https://orcid.org/0000-0003-0071-8402
Conflits d’intérêts
Les auteurs ne déclarent aucun conflit d’intérêt.
Références
- Boenink R.. The ERA Registry Annual Report 2022: Epidemiology of Kidney Replacement Therapy in Europe, with a focus on sex comparisons. Clin Kidney J. 2025; 18(2)
- Kumar V.A.. Survival of propensity matched incident peritoneal and hemodialysis patients in a United States health care system. Kidney Int. 2014; 86(5):1016-22.
- Bonenkamp A.A.. Trends in home dialysis use differ among age categories in past two decades: A Dutch registry study. Eur J Clin Invest. 2022; 52(1)
- Williams J.D.. Morphologic changes in the peritoneal membrane of patients with renal disease. J Am Soc Nephrol. 2002; 13(2):470-479.
- Davies S.J.. Peritoneal glucose exposure and changes in membrane solute transport with time on peritoneal dialysis. J Am Soc Nephrol. 2001; 12(5):1046-1051.
- Grossin N.. Improved in vitro biocompatibility of bicarbonate-buffered peritoneal dialysis fluid. Perit Dial Int. 2006; 26(6):664-70.
- Mortier S.. Benefits of switching from a conventional to a low-GDP bicarbonate/lactate-buffered dialysis solution in a rat model. Kidney Int. 2005; 67(4):1559-65.
- Mortier S.. Long-term exposure to new peritoneal dialysis solutions: Effects on the peritoneal membrane. Kidney Int. 2004; 66(3):1257-65.
- Sugiyama N.. Low-GDP, pH-neutral solutions preserve peritoneal endothelial glycocalyx during long-term peritoneal dialysis. Clin Exp Nephrol. 2021; 25(9):1035-1046.
- Nakao M.. Risk factors for encapsulating peritoneal sclerosis: Analysis of a 36-year experience in a University Hospital. Nephrology (Carlton. 2017; 22(11):907-912.
- Nakayama M.. Pathophysiology of encapsulating peritoneal sclerosis: lessons from findings of the past three decades in Japan. Clin Exp Nephrol. 2023; 27(9):717-727.
- Cho Y.. The impact of neutral-pH peritoneal dialysates with reduced glucose degradation products on clinical outcomes in peritoneal dialysis patients. Kidney Int. 2013; 84(5):969-79.
- Htay H.. Biocompatible dialysis fluids for peritoneal dialysis. Cochrane Database Syst Rev. 2018; 10(10)
- Yohanna S.. Effect of Neutral-pH, Low-Glucose Degradation Product Peritoneal Dialysis Solutions on Residual Renal Function, Urine Volume, and Ultrafiltration: A Systematic Review and Meta-Analysis. Clin J Am Soc Nephrol. 2015; 10(8):1380-8.
- Schaefer B.. Neutral pH and low-glucose degradation product dialysis fluids induce major early alterations of the peritoneal membrane in children on peritoneal dialysis. Kidney Int. 2018; 94(2):419-429.
- Grodstein G.P.. Glucose absorption during continuous ambulatory peritoneal dialysis. Kidney Int. 1981; 19(4):564-7.
- Kotla S.K., Saxena A., Saxena R.. A Model To Estimate Glucose Absorption in Peritoneal Dialysis: A Pilot Study. Kidney360. 2020; 1(12):1373-1379.
- Poole C.Y.. NEPP" peritoneal dialysis regimen has beneficial effects on plasma CEL and 3-DG, but not pentosidine, CML, and MGO. Perit Dial Int. 2012; 32(1):45-54.
- Zeier M.. Glucose degradation products in PD fluids: do they disappear from the peritoneal cavity and enter the systemic circulation?. Kidney Int. 2003; 63(1):298-305.
- Krediet R.T.. Physiology of peritoneal dialysis; pathophysiology in long-term patients. Front Physiol. 2024; 15
- Krediet R.T., Parikova A.. Relative Contributions of Pseudohypoxia and Inflammation to Peritoneal Alterations with Long-Term Peritoneal Dialysis Patients. Clin J Am Soc Nephrol. 2022; 17(8):1259-1266.
- Krediet R.T., Parikova A.. Glucose-induced pseudohypoxia and advanced glycosylation end products explain peritoneal damage in long-term peritoneal dialysis. Perit Dial Int. 2024; 44(1):6-15.
- Dioos B.. Biocompatibility of a new PD solution for Japan, Reguneal, measured as in vitro proliferation of fibroblasts. Clin Exp Nephrol. 2018; 22(6):1427-1436.
- Sun T.. Excessive salt intake increases peritoneal solute transport rate via local tonicity-responsive enhancer binding protein in subtotal nephrectomized mice. Nephrol Dial Transplant. 2019; 34(12):2031-2042.
- Seeger H.. The potential role of NFAT5 and osmolarity in peritoneal injury. Biomed Res Int. 2015.
- Kuper C., Beck F.X., Neuhofer W.. NFAT5 contributes to osmolality-induced MCP-1 expression in mesothelial cells. Mediators Inflamm. 2012.
- Goossen K.. Icodextrin Versus Glucose Solutions for the Once-Daily Long Dwell in Peritoneal Dialysis: An Enriched Systematic Review and Meta-analysis of Randomized Controlled Trials. Am J Kidney Dis. 2020; 75(6):830-846.
- Lin A.. Randomized controlled trial of icodextrin versus glucose containing peritoneal dialysis fluid. Clin J Am Soc Nephrol. 2009; 4(11):1799-804.
- Moraes T.P.. Icodextrin reduces insulin resistance in non-diabetic patients undergoing automated peritoneal dialysis: results of a randomized controlled trial (STARCH. Nephrol Dial Transplant. 2015; 30(11):1905-11.
- Li P.K.. Randomized, controlled trial of glucose-sparing peritoneal dialysis in diabetic patients. J Am Soc Nephrol. 2013; 24(11):1889-900.
- Reimann D.. Amino acid-based peritoneal dialysis solution stimulates mesothelial nitric oxide production. Perit Dial Int. 2004; 24(4):378-84.
- Tjiong H.L.. Dialysate as food: combined amino acid and glucose dialysate improves protein anabolism in renal failure patients on automated peritoneal dialysis. J Am Soc Nephrol. 2005; 16(5):1486-93.
- Holmes C.J., Shockley T.R.. Strategies to Reduce Glucose Exposure in Peritoneal Dialysis Patients. Peritoneal Dialysis International: Journal of the International Society for Peritoneal Dialysis. 2000; 20(2_suppl):37-41.
- Bonomini M.. L-carnitine is an osmotic agent suitable for peritoneal dialysis. Kidney Int. 2011; 80(6):645-54.
- Gaggiotti E.. Prevention of peritoneal sclerosis: a new proposal to substitute glucose with carnitine dialysis solution (biocompatibility testing in vitro and in rabbits. Int J Artif Organs. 2005; 28(2):177-87.
- Bonomini M.. Effect of an L-carnitine-containing peritoneal dialysate on insulin sensitivity in patients treated with CAPD: a 4-month, prospective, multicenter randomized trial. Am J Kidney Dis. 2013; 62(5):929-38.
- Bazzato G.. Xylitol as osmotic agent in CAPD: an alternative to glucose for uremic diabetic patients?. Trans Am Soc Artif Intern Organs. 1982; 28:280-6.
- Bonomini M.. Effect of peritoneal dialysis fluid containing osmo-metabolic agents on human endothelial cells. Drug Des Devel Ther. 2016; 10:3925-3932.
- Piccapane F.. A Novel Formulation of Glucose-Sparing Peritoneal Dialysis Solutions with l-Carnitine Improves Biocompatibility on Human Mesothelial Cells. Int J Mol Sci. 2020; 22(1)
- Bonomini M.. Rationale and design of ELIXIR, a randomized, controlled trial to evaluate efficacy and safety of XyloCore, a glucose-sparing solution for peritoneal dialysis. Perit Dial Int. 2025; 45(1):17-25.
- Herzog R.. Dynamic O-linked N-acetylglucosamine modification of proteins affects stress responses and survival of mesothelial cells exposed to peritoneal dialysis fluids. J Am Soc Nephrol. 2014; 25(12):2778-88.
- Bartosova M.. Alanyl-Glutamine Restores Tight Junction Organization after Disruption by a Conventional Peritoneal Dialysis Fluid. Biomolecules. 2020; 10(8)
- Ferrantelli E.. The dipeptide alanyl-glutamine ameliorates peritoneal fibrosis and attenuates IL-17 dependent pathways during peritoneal dialysis. Kidney Int. 2016; 89(3):625-35.
- Herzog R.. Peritoneal Dialysis Fluid Supplementation with Alanyl-Glutamine Attenuates Conventional Dialysis Fluid-Mediated Endothelial Cell Injury by Restoring Perturbed Cytoprotective Responses. Biomolecules. 2020; 10(12)
- Herzog R.. Functional and Transcriptomic Characterization of Peritoneal Immune-Modulation by Addition of Alanyl-Glutamine to Dialysis Fluid. Sci Rep. 2017; 7(1)
- Kratochwill K.. Addition of Alanyl-Glutamine to Dialysis Fluid Restores Peritoneal Cellular Stress Responses - A First-In-Man Trial. PLoS One. 2016; 11(10)
- Kratochwill K.. Alanyl-glutamine dipeptide restores the cytoprotective stress proteome of mesothelial cells exposed to peritoneal dialysis fluids. Nephrol Dial Transplant. 2012; 27(3):937-46.
- Vychytil A.. A randomized controlled trial of alanyl-glutamine supplementation in peritoneal dialysis fluid to assess impact on biomarkers of peritoneal health. Kidney Int. 2018; 94(6):1227-1237.
- Balzer M.S.. SGLT2 Inhibition by Intraperitoneal Dapagliflozin Mitigates Peritoneal Fibrosis and Ultrafiltration Failure in a Mouse Model of Chronic Peritoneal Exposure to High-Glucose Dialysate. Biomolecules. 2020; 10(11)
- Shentu Y.. Empagliflozin, a sodium glucose cotransporter-2 inhibitor, ameliorates peritoneal fibrosis via suppressing TGF-beta/Smad signaling. Int Immunopharmacol. 2021; 93
- Shi P.. The antioxidative effects of empagliflozin on high glucose‐induced epithelial-mesenchymal transition in peritoneal mesothelial cells via the Nrf2/HO-1 signaling. Ren Fail. 2022; 44(1):1528-1542.
- Zhou Y.. SGLT-2 inhibitors reduce glucose absorption from peritoneal dialysis solution by suppressing the activity of SGLT-2. Biomed Pharmacother. 2019; 109:1327-1338.
- Lho Y.. Empagliflozin attenuates epithelial-to-mesenchymal transition through senescence in peritoneal dialysis. Am J Physiol Renal Physiol. 2nd; 327(3):363-372.
- Martus G.. SGLT2 inhibition does not reduce glucose absorption during experimental peritoneal dialysis. Perit Dial Int. 2021; 41(4):373-380.
- Vorobiov M.. Blockade of sodium-glucose co-transporters improves peritoneal ultrafiltration in uraemic rodent models. Perit Dial Int. 2024; 44(1):48-55.
- Doi Y.. Effects of sodium-glucose co-transporter 2 inhibitors on ultrafiltration in patients with peritoneal dialysis: a protocol for a randomized, double-blind, placebo-controlled, crossover trial (EMPOWERED. Clin Exp Nephrol. 2024; 28(7):629-635.
- Pitaraki E.. 2-Deoxy-glucose ameliorates the peritoneal mesothelial and endothelial barrier function perturbation occurring due to Peritoneal Dialysis fluids exposure. Biochem Biophys Res Commun. 2024; 693
- Si M.. Inhibition of hyperglycolysis in mesothelial cells prevents peritoneal fibrosis. Sci Transl Med. 2019; 11(495)
- Herzog R.. Lithium preserves peritoneal membrane integrity by suppressing mesothelial cell alphaB-crystallin. Sci Transl Med. 2021; 13(608)
- Kopytina V.. Steviol glycosides as an alternative osmotic agent for peritoneal dialysis fluid. Front Pharmacol. 2022; 13
- Mendelson A.A.. Hyperbranched polyglycerol is an efficacious and biocompatible novel osmotic agent in a rodent model of peritoneal dialysis. Perit Dial Int. 2013; 33(1):15-27.
- Nishimura H.. Evaluation of taurine as an osmotic agent for peritoneal dialysis solution. Perit Dial Int. 2009; 29(2):204-16.
- Freida P.. The contribution of combined crystalloid and colloid osmosis to fluid and sodium management in peritoneal dialysis. Kidney Int Suppl. 2008(108):102-11.
- Leypoldt J.K.. Low-Polydispersity Glucose Polymers as Osmotic Agents for Peritoneal Dialysis. Perit Dial Int. 2015; 35(4):428-35.
- Rutkowski B.. Low-Sodium Versus Standard-Sodium Peritoneal Dialysis Solution in Hypertensive Patients: A Randomized Controlled Trial. Am J Kidney Dis. 2016; 67(5):753-61.
Références
Boenink, R., et al., The ERA Registry Annual Report 2022: Epidemiology of Kidney Replacement Therapy in Europe, with a focus on sex comparisons. Clin Kidney J, 2025. 18(2): p. sfae405. DOI: https://doi.org/10.1093/ckj/sfaf107
Kumar, V.A., et al., Survival of propensity matched incident peritoneal and hemodialysis patients in a United States health care system. Kidney Int, 2014. 86(5): p. 1016-22. DOI: https://doi.org/10.1038/ki.2014.224
Bonenkamp, A.A., et al., Trends in home dialysis use differ among age categories in past two decades: A Dutch registry study. Eur J Clin Invest, 2022. 52(1): p. e13656. DOI: https://doi.org/10.1111/eci.13656
Williams, J.D., et al., Morphologic changes in the peritoneal membrane of patients with renal disease. J Am Soc Nephrol, 2002. 13(2): p. 470-479. DOI: https://doi.org/10.1681/ASN.V132470
Davies, S.J., et al., Peritoneal glucose exposure and changes in membrane solute transport with time on peritoneal dialysis. J Am Soc Nephrol, 2001. 12(5): p. 1046-1051. DOI: https://doi.org/10.1681/ASN.V1251046
Grossin, N., et al., Improved in vitro biocompatibility of bicarbonate-buffered peritoneal dialysis fluid. Perit Dial Int, 2006. 26(6): p. 664-70. DOI: https://doi.org/10.1177/089686080602600610
Mortier, S., et al., Benefits of switching from a conventional to a low-GDP bicarbonate/lactate-buffered dialysis solution in a rat model. Kidney Int, 2005. 67(4): p. 1559-65. DOI: https://doi.org/10.1111/j.1523-1755.2005.00237.x
Mortier, S., et al., Long-term exposure to new peritoneal dialysis solutions: Effects on the peritoneal membrane. Kidney Int, 2004. 66(3): p. 1257-65. DOI: https://doi.org/10.1111/j.1523-1755.2004.00879.x
Sugiyama, N., et al., Low-GDP, pH-neutral solutions preserve peritoneal endothelial glycocalyx during long-term peritoneal dialysis. Clin Exp Nephrol, 2021. 25(9): p. 1035-1046. DOI: https://doi.org/10.1007/s10157-021-02078-9
Nakao, M., et al., Risk factors for encapsulating peritoneal sclerosis: Analysis of a 36-year experience in a University Hospital. Nephrology (Carlton), 2017. 22(11): p. 907-912. DOI: https://doi.org/10.1111/nep.12911
Nakayama, M., et al., Pathophysiology of encapsulating peritoneal sclerosis: lessons from findings of the past three decades in Japan. Clin Exp Nephrol, 2023. 27(9): p. 717-727. DOI: https://doi.org/10.1007/s10157-023-02360-y
Cho, Y., et al., The impact of neutral-pH peritoneal dialysates with reduced glucose degradation products on clinical outcomes in peritoneal dialysis patients. Kidney Int, 2013. 84(5): p. 969-79. DOI: https://doi.org/10.1038/ki.2013.190
Htay, H., et al., Biocompatible dialysis fluids for peritoneal dialysis. Cochrane Database Syst Rev, 2018. 10(10): p. CD007554. DOI: https://doi.org/10.1002/14651858.CD007554.pub3
Yohanna, S., et al., Effect of Neutral-pH, Low-Glucose Degradation Product Peritoneal Dialysis Solutions on Residual Renal Function, Urine Volume, and Ultrafiltration: A Systematic Review and Meta-Analysis. Clin J Am Soc Nephrol, 2015. 10(8): p. 1380-8. DOI: https://doi.org/10.2215/CJN.05410514
Schaefer, B., et al., Neutral pH and low-glucose degradation product dialysis fluids induce major early alterations of the peritoneal membrane in children on peritoneal dialysis. Kidney Int, 2018. 94(2): p. 419-429. DOI: https://doi.org/10.1016/j.kint.2018.02.022
Grodstein, G.P., et al., Glucose absorption during continuous ambulatory peritoneal dialysis. Kidney Int, 1981. 19(4): p. 564-7. DOI: https://doi.org/10.1038/ki.1981.53
Kotla, S.K., A. Saxena, and R. Saxena, A Model To Estimate Glucose Absorption in Peritoneal Dialysis: A Pilot Study. Kidney360, 2020. 1(12): p. 1373-1379. DOI: https://doi.org/10.34067/KID.0004722020
le Poole, C.Y., et al., "NEPP" peritoneal dialysis regimen has beneficial effects on plasma CEL and 3-DG, but not pentosidine, CML, and MGO. Perit Dial Int, 2012. 32(1): p. 45-54. DOI: https://doi.org/10.3747/pdi.2010.00101
Zeier, M., et al., Glucose degradation products in PD fluids: do they disappear from the peritoneal cavity and enter the systemic circulation? Kidney Int, 2003. 63(1): p. 298-305. DOI: https://doi.org/10.1046/j.1523-1755.2003.00705.x
Krediet, R.T., Physiology of peritoneal dialysis; pathophysiology in long-term patients. Front Physiol, 2024. 15: p. 1322493. DOI: https://doi.org/10.3389/fphys.2024.1322493
Krediet, R.T. and A. Parikova, Relative Contributions of Pseudohypoxia and Inflammation to Peritoneal Alterations with Long-Term Peritoneal Dialysis Patients. Clin J Am Soc Nephrol, 2022. 17(8): p. 1259-1266. DOI: https://doi.org/10.2215/CJN.15371121
Krediet, R.T. and A. Parikova, Glucose-induced pseudohypoxia and advanced glycosylation end products explain peritoneal damage in long-term peritoneal dialysis. Perit Dial Int, 2024. 44(1): p. 6-15. DOI: https://doi.org/10.1177/08968608231196033
Dioos, B., et al., Biocompatibility of a new PD solution for Japan, Reguneal, measured as in vitro proliferation of fibroblasts. Clin Exp Nephrol, 2018. 22(6): p. 1427-1436. DOI: https://doi.org/10.1007/s10157-018-1602-2
Sun, T., et al., Excessive salt intake increases peritoneal solute transport rate via local tonicity-responsive enhancer binding protein in subtotal nephrectomized mice. Nephrol Dial Transplant, 2019. 34(12): p. 2031-2042. DOI: https://doi.org/10.1093/ndt/gfz045
Seeger, H., et al., The potential role of NFAT5 and osmolarity in peritoneal injury. Biomed Res Int, 2015. 2015: p. 578453. DOI: https://doi.org/10.1155/2015/578453
Kuper, C., F.X. Beck, and W. Neuhofer, NFAT5 contributes to osmolality-induced MCP-1 expression in mesothelial cells. Mediators Inflamm, 2012. 2012: p. 513015. DOI: https://doi.org/10.1155/2012/513015
Goossen, K., et al., Icodextrin Versus Glucose Solutions for the Once-Daily Long Dwell in Peritoneal Dialysis: An Enriched Systematic Review and Meta-analysis of Randomized Controlled Trials. Am J Kidney Dis, 2020. 75(6): p. 830-846. DOI: https://doi.org/10.1053/j.ajkd.2019.10.004
Lin, A., et al., Randomized controlled trial of icodextrin versus glucose containing peritoneal dialysis fluid. Clin J Am Soc Nephrol, 2009. 4(11): p. 1799-804. DOI: https://doi.org/10.2215/CJN.02950509
de Moraes, T.P., et al., Icodextrin reduces insulin resistance in non-diabetic patients undergoing automated peritoneal dialysis: results of a randomized controlled trial (STARCH). Nephrol Dial Transplant, 2015. 30(11): p. 1905-11. DOI: https://doi.org/10.1093/ndt/gfv247
Li, P.K., et al., Randomized, controlled trial of glucose-sparing peritoneal dialysis in diabetic patients. J Am Soc Nephrol, 2013. 24(11): p. 1889-900. DOI: https://doi.org/10.1681/ASN.2012100987
Reimann, D., et al., Amino acid-based peritoneal dialysis solution stimulates mesothelial nitric oxide production. Perit Dial Int, 2004. 24(4): p. 378-84. DOI: https://doi.org/10.1177/089686080402400414
Tjiong, H.L., et al., Dialysate as food: combined amino acid and glucose dialysate improves protein anabolism in renal failure patients on automated peritoneal dialysis. J Am Soc Nephrol, 2005. 16(5): p. 1486-93. DOI: https://doi.org/10.1681/ASN.2004050402
Holmes, C.J. and T.R. Shockley, Strategies to Reduce Glucose Exposure in Peritoneal Dialysis Patients. Peritoneal Dialysis International: Journal of the International Society for Peritoneal Dialysis, 2000. 20(2_suppl): p. 37-41. DOI: https://doi.org/10.1177/089686080002002S08
Bonomini, M., et al., L-carnitine is an osmotic agent suitable for peritoneal dialysis. Kidney Int, 2011. 80(6): p. 645-54. DOI: https://doi.org/10.1038/ki.2011.117
Gaggiotti, E., et al., Prevention of peritoneal sclerosis: a new proposal to substitute glucose with carnitine dialysis solution (biocompatibility testing in vitro and in rabbits). Int J Artif Organs, 2005. 28(2): p. 177-87. DOI: https://doi.org/10.1177/039139880502800215
Bonomini, M., et al., Effect of an L-carnitine-containing peritoneal dialysate on insulin sensitivity in patients treated with CAPD: a 4-month, prospective, multicenter randomized trial. Am J Kidney Dis, 2013. 62(5): p. 929-38. DOI: https://doi.org/10.1053/j.ajkd.2013.04.007
Bazzato, G., et al., Xylitol as osmotic agent in CAPD: an alternative to glucose for uremic diabetic patients? Trans Am Soc Artif Intern Organs, 1982. 28: p. 280-6.
Bonomini, M., et al., Effect of peritoneal dialysis fluid containing osmo-metabolic agents on human endothelial cells. Drug Des Devel Ther, 2016. 10: p. 3925-3932. DOI: https://doi.org/10.2147/DDDT.S117078
Piccapane, F., et al., A Novel Formulation of Glucose-Sparing Peritoneal Dialysis Solutions with l-Carnitine Improves Biocompatibility on Human Mesothelial Cells. Int J Mol Sci, 2020. 22(1). DOI: https://doi.org/10.3390/ijms22010123
Bonomini, M., et al., Rationale and design of ELIXIR, a randomized, controlled trial to evaluate efficacy and safety of XyloCore, a glucose-sparing solution for peritoneal dialysis. Perit Dial Int, 2025. 45(1): p. 17-25. DOI: https://doi.org/10.1177/08968608241274106
Herzog, R., et al., Dynamic O-linked N-acetylglucosamine modification of proteins affects stress responses and survival of mesothelial cells exposed to peritoneal dialysis fluids. J Am Soc Nephrol, 2014. 25(12): p. 2778-88. DOI: https://doi.org/10.1681/ASN.2013101128
Bartosova, M., et al., Alanyl-Glutamine Restores Tight Junction Organization after Disruption by a Conventional Peritoneal Dialysis Fluid. Biomolecules, 2020. 10(8). DOI: https://doi.org/10.3390/biom10081178
Ferrantelli, E., et al., The dipeptide alanyl-glutamine ameliorates peritoneal fibrosis and attenuates IL-17 dependent pathways during peritoneal dialysis. Kidney Int, 2016. 89(3): p. 625-35. DOI: https://doi.org/10.1016/j.kint.2015.12.005
Herzog, R., et al., Peritoneal Dialysis Fluid Supplementation with Alanyl-Glutamine Attenuates Conventional Dialysis Fluid-Mediated Endothelial Cell Injury by Restoring Perturbed Cytoprotective Responses. Biomolecules, 2020. 10(12). DOI: https://doi.org/10.3390/biom10121678
Herzog, R., et al., Functional and Transcriptomic Characterization of Peritoneal Immune-Modulation by Addition of Alanyl-Glutamine to Dialysis Fluid. Sci Rep, 2017. 7(1): p. 6229. DOI: https://doi.org/10.1038/s41598-017-05872-2
Kratochwill, K., et al., Addition of Alanyl-Glutamine to Dialysis Fluid Restores Peritoneal Cellular Stress Responses - A First-In-Man Trial. PLoS One, 2016. 11(10): p. e0165045. DOI: https://doi.org/10.1371/journal.pone.0165045
Kratochwill, K., et al., Alanyl-glutamine dipeptide restores the cytoprotective stress proteome of mesothelial cells exposed to peritoneal dialysis fluids. Nephrol Dial Transplant, 2012. 27(3): p. 937-46. DOI: https://doi.org/10.1093/ndt/gfr459
Vychytil, A., et al., A randomized controlled trial of alanyl-glutamine supplementation in peritoneal dialysis fluid to assess impact on biomarkers of peritoneal health. Kidney Int, 2018. 94(6): p. 1227-1237. DOI: https://doi.org/10.1016/j.kint.2018.08.031
Balzer, M.S., et al., SGLT2 Inhibition by Intraperitoneal Dapagliflozin Mitigates Peritoneal Fibrosis and Ultrafiltration Failure in a Mouse Model of Chronic Peritoneal Exposure to High-Glucose Dialysate. Biomolecules, 2020. 10(11). DOI: https://doi.org/10.3390/biom10111573
Shentu, Y., et al., Empagliflozin, a sodium glucose cotransporter-2 inhibitor, ameliorates peritoneal fibrosis via suppressing TGF-beta/Smad signaling. Int Immunopharmacol, 2021. 93: p. 107374. DOI: https://doi.org/10.1016/j.intimp.2021.107374
Shi, P., et al., The antioxidative effects of empagliflozin on high glucose‑induced epithelial-mesenchymal transition in peritoneal mesothelial cells via the Nrf2/HO-1 signaling. Ren Fail, 2022. 44(1): p. 1528-1542. DOI: https://doi.org/10.1080/0886022X.2022.2118066
Zhou, Y., et al., SGLT-2 inhibitors reduce glucose absorption from peritoneal dialysis solution by suppressing the activity of SGLT-2. Biomed Pharmacother, 2019. 109: p. 1327-1338. DOI: https://doi.org/10.1016/j.biopha.2018.10.106
Lho, Y., 2nd, et al., Empagliflozin attenuates epithelial-to-mesenchymal transition through senescence in peritoneal dialysis. Am J Physiol Renal Physiol, 2024. 327(3): p. F363-F372. DOI: https://doi.org/10.1152/ajprenal.00028.2024
Martus, G., et al., SGLT2 inhibition does not reduce glucose absorption during experimental peritoneal dialysis. Perit Dial Int, 2021. 41(4): p. 373-380. DOI: https://doi.org/10.1177/08968608211008095
Vorobiov, M., et al., Blockade of sodium-glucose co-transporters improves peritoneal ultrafiltration in uraemic rodent models. Perit Dial Int, 2024. 44(1): p. 48-55. DOI: https://doi.org/10.1177/08968608231165865
Doi, Y., et al., Effects of sodium-glucose co-transporter 2 inhibitors on ultrafiltration in patients with peritoneal dialysis: a protocol for a randomized, double-blind, placebo-controlled, crossover trial (EMPOWERED). Clin Exp Nephrol, 2024. 28(7): p. 629-635. DOI: https://doi.org/10.1007/s10157-024-02467-w
Pitaraki, E., et al., 2-Deoxy-glucose ameliorates the peritoneal mesothelial and endothelial barrier function perturbation occurring due to Peritoneal Dialysis fluids exposure. Biochem Biophys Res Commun, 2024. 693: p. 149376. DOI: https://doi.org/10.1016/j.bbrc.2023.149376
Si, M., et al., Inhibition of hyperglycolysis in mesothelial cells prevents peritoneal fibrosis. Sci Transl Med, 2019. 11(495). DOI: https://doi.org/10.1126/scitranslmed.aav5341
Herzog, R., et al., Lithium preserves peritoneal membrane integrity by suppressing mesothelial cell alphaB-crystallin. Sci Transl Med, 2021. 13(608). DOI: https://doi.org/10.1126/scitranslmed.aaz9705
Kopytina, V., et al., Steviol glycosides as an alternative osmotic agent for peritoneal dialysis fluid. Front Pharmacol, 2022. 13: p. 868374. DOI: https://doi.org/10.3389/fphar.2022.868374
Mendelson, A.A., et al., Hyperbranched polyglycerol is an efficacious and biocompatible novel osmotic agent in a rodent model of peritoneal dialysis. Perit Dial Int, 2013. 33(1): p. 15-27. DOI: https://doi.org/10.3747/pdi.2012.00148
Nishimura, H., et al., Evaluation of taurine as an osmotic agent for peritoneal dialysis solution. Perit Dial Int, 2009. 29(2): p. 204-16. DOI: https://doi.org/10.1177/089686080902900216
Freida, P., et al., The contribution of combined crystalloid and colloid osmosis to fluid and sodium management in peritoneal dialysis. Kidney Int Suppl, 2008(108): p. S102-11. DOI: https://doi.org/10.1038/sj.ki.5002610
Leypoldt, J.K., et al., Low-Polydispersity Glucose Polymers as Osmotic Agents for Peritoneal Dialysis. Perit Dial Int, 2015. 35(4): p. 428-35. DOI: https://doi.org/10.3747/pdi.2013.00232
Rutkowski, B., et al., Low-Sodium Versus Standard-Sodium Peritoneal Dialysis Solution in Hypertensive Patients: A Randomized Controlled Trial. Am J Kidney Dis, 2016. 67(5): p. 753-61. DOI: https://doi.org/10.1053/j.ajkd.2015.07.031
Téléchargements
Soumis
Accepté
Publié
Comment citer
Numéro
Rubrique
Licence
© Celeste Smeys, Freya Van Hulle, 2025

Ce travail est disponible sous la licence Creative Commons Attribution 4.0 International .










